Átdolgozásával élettani folyamatok(6.6; 7.2.5. fejezetek; 9. fejezet), amelyek a farmakokinetikai paramétereket meghatározzák, megadtuk azok jellemzőit. Az anyag jobb megértése érdekében a fenti paraméterek közül néhányat megismételünk, és néhányat először veszünk figyelembe.
Az eliminációs sebesség állandó (megnevezése - Ke1, dimenzió - h-1, min-1) egy olyan paraméter, amely a hatóanyagnak a kiválasztás és biotranszformáció révén történő eliminációjának sebességét jellemzi. A többrészes modellekben a Ke1 érték általában a gyógyszer kiürülését jellemzi a központi kamrából, amely vért és szöveteket foglal magában, amelyek gyorsan kicserélik a gyógyszert a vérrel. A gyógyszer szervezetből való eliminációját ebben az esetben a látszólagos eliminációs állandó jellemzi - egy összetett paraméter (jelölés P, dimenzió - h-1, min-1), amely a modell egyéb állandóihoz kapcsolódik (Kір, lásd alább).
A felszívódási (abszorpciós) sebességi állandó (jelölése K01, dimenzió - h-1) egy olyan paraméter, amely az injekció beadásának helyéről a szisztémás keringésbe jutásának sebességét jellemzi az extravascularis beadási mód során.
A gyógyszer részek (kamrák) közötti átmenetének sebességi állandója többrészes (többkamrás) modellekben (Kf dimenzió - h-1, min-1) egy olyan paraméter, amely jellemzi a gyógyszer kibocsátásának sebességét i-edik kamrából az i-edik kamrába Például egy kétrészes modellben két átmeneti sebességi állandó van – az egyik a központi (első kamra) a perifériásba (második) való átmenet sebességét jellemzi, és a /. C,2; fordított folyamatés a K2X jelzésű. Ezen állandók aránya határozza meg a gyógyszer egyensúlyi eloszlását. Összességében a két kamra közötti eloszlási folyamat kinetikáját egy összetett paraméter jellemzi, amely a modell által figyelembe vett összes folyamat sebességi állandójától függ. A kétrészes modell keretein belül ezt a paramétert a-val jelöljük, mérete h-1, min-1.
A kiválasztási sebesség állandó (Ke vagy Keh jelölése, dimenzió - h-1, min-1) a gyógyszer kiválasztódási sebességét jellemző paraméter bármilyen kiválasztódás esetén: vizelet, széklet, nyál, tej stb. A lineáris kereten belül A modell szerint ennek az állandónak nagyságrendileg egybe kell esnie az eliminációs sebességi állandóval, ha a gyógyszer csak egyetlen módon, változatlan formában, például vizelettel ürül ki a szervezetből. Más esetekben a Kex értéke egyenlő a Ke1- törtével
A gyógyszer félkiürülési periódusa (jelölése Tx/2, méret - h, min) a beadott és kapott gyógyszeradag felének a szervezetből történő eliminációjának ideje. Megfelel annak az időnek, amikor a gyógyszer koncentrációja felére csökken a vérplazmában (szérumban) a gyógyszer plazma (szérum) szintjének monoexpotenciális csökkenésének helyén, azaz a P-fázisban.
A T|/2 értékét a gyógyszer teljes kiválasztódása és biotranszformációja, azaz eliminációja határozza meg. A felezési idő egyedileg függ az eliminációs sebességi állandótól: egyrészes modellnél - T1/2 = 0,693/Keh többrészes modellnél - T1/2 - 0,693/r.
A gyógyszer félfelszívódási (félfelszívódási) periódusa (Tx/2a jelölés, dimenzió - h, min) az az idő, amely a beadott dózis felének az injekció helyéről a szisztémás keringésbe történő felszívódásához (felszívódáshoz) szükséges. A paraméter a gyógyszer kinetikáját írja le extravaszkuláris adagolás esetén, és egyértelműen függ a gyógyszer felszívódás sebességi állandójától.
A gyógyszer felezési ideje (jelölése Tx/2a, dimenzió - h, min) egy feltételes paraméter, amely egy kétrészes modell keretein belül jellemzi a központi kamra, beleértve a vérplazmát, és a perifériás kamra közötti eloszlást. kamra (szervek, szövetek). A Tx/2a érték annak az időnek felel meg, amely a vér és más szövetek közötti egyensúly elérésekor megfigyelt egyensúlyi koncentráció 50%-ának megfelelő gyógyszerszint eléréséhez szükséges.
A gyógyszer látszólagos kezdeti koncentrációja (jelölése C0 vagy C°, dimenzió - mmol/l, μg/l, ng/ml stb.) egy feltételes paraméter, amely megegyezik azzal a koncentrációval, amelyet a vérplazmában kapnánk, ha a gyógyszert bekerült a vérbe és azonnali eloszlása a szervek és szövetek között (egyrészes modell elemzésekor), vagy a központi kamra térfogatában (két- és többrészes modellek elemzésekor). A gyógyszer lineáris kinetikájával rendelkező C értéke a szervezetben egyenesen arányos a gyógyszer dózisával.
A gyógyszer stacionárius koncentrációja a vérplazmában (jelölése Css, dimenzió - mmol/l, μg/l, ng/ml) az a koncentráció, amely a vérplazmában (szérumban) akkor alakul ki, amikor a gyógyszer állandó értéken kerül a szervezetbe. mérték.
Egy gyógyszer egyenlő időközönként, egyenlő dózisokban történő szakaszos beadása (beadása) esetén a maximális egyensúlyi koncentráció (C™x) és a minimális egyensúlyi koncentráció (C™p) fogalmát alkalmazzuk.
A gyógyszer eloszlási térfogata (jelölése Vd vagy V, dimenzió - l, ml) egy feltételes paraméter, amely a szövetek vérplazmából (szérumból) történő gyógyszerfelvételének mértékét jellemzi. A Vd értéke egy egyrészes modell keretein belül egyenlő azzal a feltételes folyadéktérfogattal, amelyben a szervezetbe jutó gyógyszer teljes dózisa eloszlik úgy, hogy a látszólagos kezdeti koncentrációval (C0) megegyező koncentrációt kapjunk. Az eloszlási térfogatot gyakran a beteg testtömegének egységére (G, kg) utalják, és megkapják a fajlagos eloszlási térfogatot (Ad megnevezés, méret - l/kg, ml/g). A többrészes modellekben az i-edik kamrában való eloszlási térfogat fogalmát vezetik be (Vh dimenzió megjelölése - l, ml). Például egy kétrészes modell elemzésekor a vérplazmát tartalmazó első, központi kamra (1/) térfogatát számítjuk ki. Az ilyen modellekben a teljes vagy kinetikai megoszlási térfogat (jelölés V$, dimenzió - l, ml) jellemzi a gyógyszer eloszlását, miután elérte a kvázi-stacionárius egyensúlyi állapotot a gyógyszer vérbeli koncentrációja (központi kamra) és egyéb szövetek (perifériás kamrák). Kétrészes modell esetén a Kp = (kei/$)/Vu kifejezés érvényes Ennél a modellnél a stacionárius eloszlási térfogat (jelölés Vss, dimenzió - l, ml) paraméter használata is. arányos az első kamra eloszlási térfogatának értékével.
Az eloszlás mennyiségét gyakran „látszólagosnak” nevezik, ami csak bonyolítja a terminológiát, de nem ad további pontosítást, mivel ennek a paraméternek a konvenciója a definíciójából következik.
A gyógyszer általános clearance-e (szinonimák: test clearance, plazma (szérum) clearance, plazma (szérum) clearance; jelölés C1 vagy C1T, méret - ml/perc, l/óra) - a tesztszövet felszabadult térfogatának megfelelő paraméter a gyógyszertől időegységben. A legegyszerűbb esetben a gyógyszer-clearance az összes lehetséges úton történő elimináció sebességének és a hatóanyag biológiai szövetekben való koncentrációjának aránya.
A gyógyszer renális (renális) clearance-e (jelölése C/renalis, Clr, ClR, méret - l/h, ml/perc) egy olyan paraméter, amely meghatározza a hatóanyagnak a szervezetből történő eliminációjának sebességét a vesén keresztül történő kiválasztódása révén. A C1G érték (feltételesen) az eloszlási térfogat azon részének felel meg, amelyből a gyógyszer egységnyi idő alatt a vizelettel ürül.
A gyógyszer extrarenális (extrarenális) clearance-e (jelölése C1en S/v/ren, C1t, méret - l/h, ml/perc) olyan paraméter, amely a kiválasztáson túlmenően a hatóanyag szervezetből történő, más úton történő eliminációjának sebességét jellemzi. a vizeletben, főként a gyógyszer biotranszformációja (metabolizmusa) és az epével történő kiválasztódása miatt. A C1er értéke (feltételesen) az eloszlási térfogat azon részének felel meg, amelyből a gyógyszer egységnyi idő alatt összesen valamennyi eliminációs útvonalon eliminálódik, kivéve a vesén keresztül történő kiválasztódást.
A koncentráció-idő görbe alatti terület (szinonimája - a farmakokinetikai görbe alatti terület; AUC vagy S jelölés, méret - mmol-h-l-1, mmol-perc-l-1, µg-h-ml-1, µg-min -ml_1 , ng-h-ml-1, ng min-ml-1 stb.) - a grafikonon koordinálja a gyógyszer koncentrációját a vérplazmában (szérumban), Cp - a gyógyszer beadása utáni idő, G, terület a farmakokinetikai görbe és a koordinátatengelyek által határolt ábra. Az AUC egy másik farmakokinetikai paraméterhez, az eloszlási térfogathoz kapcsolódik; Az AUC fordítottan arányos a gyógyszer teljes clearance-ével. Ha a gyógyszer kinetikája a szervezetben lineáris, akkor az AUC érték arányos a szervezetbe kerülő gyógyszer teljes mennyiségével (dózisával). Gyakran nem a teljes farmakokinetikai görbe alatti területet használják (nullától az időben végtelenig), hanem a görbe egy része alatti területet (nullától bizonyos t időpontig)\ ezt a paramétert az AUC jelöli.
Ideje elérni maximális koncentráció(megjelölés £max vagy /max, méret - h, min) - a gyógyszer koncentrációjának elérésének ideje a vérben.
Bisoprolol
| Információ a TKFS-től | |
| Biohasznosulás, % | 70% |
| Az élelmiszer hatása a felszívódásra | Nem befolyásolja az adszorpciót |
| 2-4 óra múlva | |
| 26-33% | |
| Eloszlási térfogat, l/kg | 3,5 l/kg |
| _ | |
| Aktív metabolitok | - |
| 9-12 óra | |
| Kiválasztó szervek | Vese |
| Clearance, ml/perc | 15 l/h |
| 50% - vesék 2% - epe | |
| Az anyatejbe kiválasztódik | |
| Kis mértékben behatol | |
Cardiomagnyl
| Farmakokinetikai paraméter | Információ a TKFS-től |
| Biohasznosulás, % | 80-100% |
| Az élelmiszer hatása a felszívódásra | Lelassul |
| A maximális koncentráció kialakulásának ideje (Tmax), h | 3 óra |
| Kommunikáció a fehérjékkel vérplazma, % | 90% |
| Eloszlási térfogat, l/kg | 170 ml/kg |
| Az anyagcserében részt vevő citokróm P-450 izoenzimek | |
| Első áthaladási hatás (máj clearance) | |
| Aktív metabolitok | |
| Felezési idő, T 1/2, h | Körülbelül 15 perc |
| Kiválasztó szervek | Vesék, belek |
| Clearance, ml/perc | |
| A gyógyszer %-a változatlan formában ürül ki | |
| Behatolás anyatej | Elég jól behatol |
| Áthatolás hisztohematikus akadályok | Behatol |
Meldonium
| Farmakokinetikai paraméter | Információ a TKFS-től |
| Biohasznosulás, % | 78% |
| Az élelmiszer hatása a felszívódásra | Gátolja az adszorpciót |
| A maximális koncentráció kialakulásának ideje (Tmax), h | 1-2 óra |
| Kapcsolódás a vérplazmafehérjékhez, % | |
| Eloszlási térfogat, l/kg | |
| Az anyagcserében részt vevő citokróm P-450 izoenzimek | |
| Első áthaladási hatás (máj clearance) | |
| Aktív metabolitok | |
| Felezési idő, T 1/2, h | 4 óra |
| Kiválasztó szervek | Vese |
| Clearance, ml/perc | |
| A gyógyszer %-a változatlan formában ürül ki | |
| Az anyatejbe jutás | Részleges |
| Behatolás hisztohematikus gátakon | Részleges |
Valzartan
| Farmakokinetikai paraméter | Információ a TKFS-től |
| Biohasznosulás, % | 25% |
| Az élelmiszer hatása a felszívódásra | 40-50%-kal csökken |
| A maximális koncentráció kialakulásának ideje (Tmax), h | 1-2 óra |
| Kapcsolódás a vérplazmafehérjékhez, % | 95% |
| Eloszlási térfogat, l/kg | 16-17 |
| Az anyagcserében részt vevő citokróm P-450 izoenzimek | Nem |
| Első áthaladási hatás (máj clearance) | |
| Aktív metabolitok | - |
| Felezési idő, T 1/2, h | 6-7 óra |
| Kiválasztó szervek | Belek, vesék |
| Clearance, ml/perc | |
| A gyógyszer %-a változatlan formában ürül ki | 70% belek, 30% vesék |
| Az anyatejbe jutás | Hiányzó adatok |
| Behatolás hisztohematikus gátakon | - |
Minden gyógyszer esetében indokolja választását. dózisforma, beadási mód, adagolási rend. Jelezze, hogy figyelembe kell-e venni a táplálékfelvételt ezekkel a gyógyszerekkel végzett farmakoterápia során. Indokolja meg az adagolási rend vagy a beteg étrendjének szükséges módosításait az Ön által felírt gyógyszeres kezeléshez.
Adagolási rendek:
Bisoprolol- 10 mg/nap, a tablettákat szájon át kell bevenni rágás nélkül, anélkül nagy mennyiség folyadékok. A bisoprololt ajánlott reggel éhgyomorra vagy reggeli közben bevenni.
Varsarta n-80 mg naponta 1 alkalommal. A tablettákat szájon át kell bevenni, étkezéstől függetlenül.
Cardiomagnyl- 75 mg naponta egyszer. A tablettákat egészben, bő vízzel kell lenyelni.
Meldonium- IV (5-10 ml oldatos injekció 0,5 g/5 ml koncentrációban), alkalmazási gyakoriság 1-2 alkalommal/nap.
11. Határozza meg minden felírt gyógyszeres kezelés időtartamát gyógyszerek. Indokolja választását (beleértve a nemzeti és nemzetközi ajánlásokon és iránymutatásokon alapuló bizonyítékok szintjének értékelését).
A farmakoterápia időtartama
Bisoprolol- A kezelés folyamata hosszú.
Valzartan- a kezelés időtartama hosszú.
Cardiomagnyl– Érvényes hosszú idő, a kúrák között (2 hónap), szünetet (1 hónap), majd ismételjen meg egy kúrát. A kezelés időtartamát az orvos egyénileg határozza meg, a betegség klinikájától, indikációitól és súlyosságától függően.
Meldonium- A kezelés időtartama 1-1,5 hónap.
12 . Készítsen programot a felírt beteg hatékonyságának értékelésére gyógyszerek(3. táblázat). Ha ez a hatékonyság értékeléséhez szükséges, indokolja meg a terápiás gyógyszermonitorozás szükségességét, jelezze a gyógyszerkoncentráció terápiás tartományát. Figyelembe kell venni, hogy ugyanaz a gyógyszer több javallatra is felírható egy betegnek. Az alábbiakban a 3. táblázat kitöltése után jelezze! lehetséges okok az előírt gyógyszeres terápia hatástalansága, javasoljon módszereket annak leküzdésére.
1. RÉSZ. A KLINIKAI FARMAKOKINETIKÁK ÁLTALÁNOS KÉRDÉSEI 1. FEJEZET FŐ FARMAKOKINEETIKAI PARAMÉTEREK ÉS KLINIKAI JELENTŐSÉGÜK
1. RÉSZ. A KLINIKAI FARMAKOKINETIKÁK ÁLTALÁNOS KÉRDÉSEI 1. FEJEZET FŐ FARMAKOKINEETIKAI PARAMÉTEREK ÉS KLINIKAI JELENTŐSÉGÜK
G.V. Ramenszkaja
A farmakoterápia célja a kívánt elérése terápiás hatás minimális mellékhatások. A „racionális gyógyszerhasználat” fogalma magában foglalja mind a szükséges gyógyszer kiválasztását, mind a dózisának meghatározását. Racionális megközelítés a farmakodinamika és a farmakodinamika elveinek kombinálása.
makokinetika, és ha a farmakodinamika jellemzi a „koncentráció-hatás” összefüggést, akkor a farmakokinetika a dózis és a koncentráció kapcsolatát vizsgálja.
Egy gyógyszer „standard” dózisa, definíció szerint klinikai vizsgálatok, egy átlagos érték, amely fiziológiai, kóros és egyéb tényezők miatt nem minden beteg számára megfelelő, ezért a farmakokinetikai és alapvető farmakokinetikai paraméterek ismerete szükséges egyéni megközelítés a gyógyszer és az adagolás kiválasztásakor.
Klinikai farmakokinetika - szakasz klinikai farmakológia, a kábítószerek emberi szervezetbe jutásának, eloszlásának, biotranszformációjának és kiválasztódásának útjait tanulmányozza.
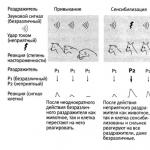
A gyógyszer hatását meghatározó egyik fő tényező a koncentrációja a receptor területén. Ennek a koncentrációnak a meghatározása meglehetősen nehéz, ezért a gyakorlatban a szervezetben a gyógyszerekkel fellépő folyamatok leírására a vérplazmában lévő gyógyszerkoncentráció értékeket használják. A gyógyszer mozgását a szervezetben általában egy farmakokinetikai görbe formájában ábrázolják, amely a gyógyszer (vagy metabolitja) vérplazmában lévő koncentrációjának a gyógyszer beadása utáni időponttól való függését ábrázolja (1. ábra). 1).
Rizs. 1-1. Farmakokinetikai görbe: 1 - felszívódású adagolási forma; 2 - intravénás beadásra szánt adagolási formához
A szervezetben zajló gyógyszereloszlási folyamatok kvantitatív értékeléséhez a farmakokinetikai matematikai leírást alkalmazzák, amely lehetővé teszi, hogy a testet egy vagy több permeábilis membránnal elkülönített rész (kamra) formájában képzeljük el, amelyben a gyógyszer eloszlik és átmegy egyik kamrából a másikba. A „kamra” fogalma önkényes, mivel nincs mögötte anatómiailag korlátozott tér. Ezt a fajta modellezést kamramodellezésnek nevezik. A központi kamrának általában a vérplazmát, annak alkotóelemeit és a jól perfúziós szerveket (szív, tüdő, máj, vese, belső elválasztású mirigyek); perifériás - rosszul perfundált szervek és szövetek (izmok, bőr, zsírszövet) számára. Ezekben a kamrákban a gyógyszert elosztják különböző sebességgel: gyorsabb a központi és lassabb a perifériás. A legegyszerűbb az egykamrás modell. Ebben az esetben feltételezzük, hogy a gyógyszer beadása után koncentrációja monoexponenciális törvény szerint csökken. A lineáris kinetika törvényeinek megfelelően egy kamrában a gyógyszer mennyiségének változási sebessége arányos a kamrában lévő mennyiségével.
Fő klinikailag jelentős farmakokinetikai paraméterek
Az adagolási rend kiválasztásakor a legfontosabb farmakokinetikai paraméterek a clearance (a szervezet gyógyszerkiürítési képességének mértéke) és a megoszlási térfogat (a szervezetben a gyógyszer befogadására alkalmas látszólagos tér mértéke).
Elosztási mennyiség Vd(l, l/kg) - a teljes gyógyszermennyiség (beadott dózis) egyenletes eloszlásához szükséges testfolyadék hipotetikus térfogata a vérplazmában lévő koncentrációhoz hasonló koncentrációban. Nál nél intravénás beadás:
 ahol C 0 a gyógyszer kezdeti koncentrációja a vérben.
ahol C 0 a gyógyszer kezdeti koncentrációja a vérben.
A nagy eloszlási térfogatértékek azt jelzik, hogy a gyógyszer aktívan behatol biológiai folyadékokés szövetek. Ha egy gyógyszert aktívan megköt például zsírszövet, annak koncentrációja a vérben szinte azonnal nagyon megnőhet.
alacsony, és az eloszlási térfogat eléri a több száz litert, ami meghaladja a testnedvek tényleges térfogatát. Ebben a tekintetben „látszólagos eloszlási térfogatnak” is nevezik. Az eloszlási térfogat attól függ különféle tényezők: a gyógyszer fizikai és kémiai tulajdonságai (molekulatömeg, ionizációs és polaritási szint, vízben és zsírokban való oldhatóság), fiziológiai tényezők (életkor, nem, a szervezetben lévő összes zsír mennyisége). Például időseknél és újszülötteknél az eloszlási térfogat csökken. A megoszlási térfogat megváltozik egyes kóros állapotokban, különösen máj-, vese-, a szív-érrendszer stb.
Az eloszlási térfogatot az adagolási rend kiválasztásakor használják az ND (telítő dózis) kiszámításához, amely szükséges a gyógyszer szükséges koncentrációjának eléréséhez a vérben:
Ahol VAL VEL- a gyógyszerek hatékony koncentrációja a vérben.
Teljes Cl clearance(ml/perc, l/h) - a plazma vagy vér térfogata, amely időegység alatt teljesen megtisztult a gyógyszertől. A lineáris modellen belül:
Tekintettel arra, hogy az elimináció fő módja a vese és a máj, a teljes clearance a vese és a máj clearance-einek összege. A hepatikus clearance a májban zajló metabolikus clearance-re és a gyógyszer epével történő kiválasztódására utal. Például, vese clearance A cimetidin körülbelül 600 ml/perc, a metabolikus - 200 ml/perc és az epeúti - 10 ml/perc, ezért a teljes clearance 810 ml/perc. Az egyéb eliminációs vagy extrahepatikus metabolizmusnak nincs jelentős gyakorlati jelentősége, és általában nem veszik figyelembe a teljes clearance kiszámításakor.
A clearance-t meghatározó fő fiziológiai tényezők a következők: funkcionális állapot a szervezet főbb élettani rendszerei, a véráramlás térfogata és a véráramlás sebessége a szervben. Sütőhöz
Egyik clearance-t sem a máj véráramlásának sebessége vagy a metabolizáló enzimek funkcionális kapacitása határozza meg. Például a májenzimek által nagymértékben metabolizálódó lidokain clearance-e elsősorban a májba való bejuttatás sebességétől függ, pl. a bejövő vér mennyiségére, a véráramlás sebességére. Ez az oka annak, hogy a lidokain clearance-e csökken, ha a máj véráramlása pangásos szívelégtelenség következtében csökken. Ugyanakkor a fenotiazinok clearance-e főként a metabolizáló enzimek funkcionális állapotától függ, ezért a hepatociták károsodása esetén a gyógyszerek clearance-e meredeken csökken, és koncentrációjuk a vérben jelentősen megnő.
Eliminációs sebesség állandó kel(h -1) - egy anyag koncentrációjának százalékos csökkenése időegység alatt (a szervezetből időegység alatt kiürülő gyógyszer arányát tükrözi).
A teljes kiürülést, a megoszlási térfogatot és az eliminációs állandót a következő egyenlet kapcsolja össze:
Felezési idő T l/2 h) - a plazmakoncentráció 50%-os csökkentéséhez szükséges idő:
Majdnem egy felezési idő alatt a gyógyszer 50% -a eliminálódik a szervezetből, két időszakban - 75%, három időszakban - körülbelül 87% stb.
A felezési idő és az eliminációs sebességi állandó kapcsolata fontos a dózisok közötti intervallum megválasztásához, valamint az egyensúlyi koncentráció eléréséhez szükséges időtartam meghatározásához (általában 5-7 T l/2) gyógyszerek ismételt beadásával.
Ha egy gyógyszert állandó dózisban, meghatározott időközönként, rövidebb időközönként adnak be, mint a gyógyszer eliminációs ideje, akkor koncentrációja a vérben nő, majd eljön egy időszak, amikor minden egyes intervallumban a következő gyógyszeradagok bevétele között. , a felszívódott gyógyszer mennyisége megegyezik az eliminált mennyiséggel. Ezt az állapotot "stacionáriusnak", ill Állandó állapotés elérte a koncentrációt
ugyanakkor - „stacionárius” (ritkábban - „egyensúly”), - Css. Ennek eredményeként a gyógyszerkoncentráció az átlagos értéken belül ingadozik, bizonyos maximumokkal (Cssmax)és minimális értékeket (Cssmin) gyógyszerkoncentrációk.
A stacionárius koncentráció megállapítása esetén a gyógyszer klinikai hatása teljes mértékben megnyilvánul. Minél rövidebb egy vegyület felezési ideje, annál hamarabb jön létre az egyensúlyi koncentráció, és annál hangsúlyosabbak lesznek az ingadozásai. Például a prokainamid felezési ideje körülbelül 2-3 óra, egyensúlyi koncentrációját pedig 6 óránkénti adagolás esetén az értékek nagy eltérése jellemzi, ezért a vér egyensúlyi koncentrációjának ezen ingadozásainak megelőzésére és csökkentésére. ban ben Utóbbi időben Egyre gyakrabban használnak nyújtott hatóanyag-leadású készítményeket.
A gyakorlatban a koncentrációból számítható ki egy gyógyszer egyensúlyi koncentrációja ezt a gyógyszert egyetlen injekció beadása után:
ahol τ a dózisok közötti időintervallum.
A vérben a szükséges gyógyszerkoncentráció fenntartásához szükséges dózis, az úgynevezett fenntartó dózis kiszámításakor a clearance értéket használják:
Ha a gyógyszert extravascularisan adják be természetes okokból nem jut el minden mennyisége a szisztémás véráramba.
Biohasznosulás F(%) - a gyógyszeradag azon része, amely az extravaszkuláris beadás után a szisztémás véráramba jut.
A biológiai hozzáférhetőség lehet abszolút vagy relatív, és a „görbe alatti terület” értékek arányaként definiálható. (AUC). Ha egy gyógyszer extravaszkuláris adagolására vonatkozó adatokat összehasonlítjuk ugyanazon gyógyszer intravénásan beadott adataival, abszolút biohasznosulást kapunk:
Ha két extravaszkuláris beadási módot hasonlítanak össze, akkor relatív biohasznosulásról beszélnek (további részletekért lásd a "Bioekvivalencia vizsgálatok").
Meg kell jegyezni, hogy a gyakorlatban az orvosnak általában nem kell kiszámítania a fő farmakokinetikai paraméterek értékeit, mivel azokat a gyógyszer használati utasításában (valamint a különböző referenciakönyvekben) adják meg. a gyógyszerről). Az orvosnak azonban képesnek kell lennie arra, hogy ezeket az adagolási rendet helyesen válassza ki egy adott beteg számára a farmakoterápia hatékonyságának és biztonságosságának növelése érdekében (1. táblázat).
Asztal 1. A fő farmakokinetikai paraméterek klinikai jelentősége
 Lent egy lehetséges eset a farmakokinetikai paraméterek ismeretének felhasználásával az adagolási rend kiszámításához.
Lent egy lehetséges eset a farmakokinetikai paraméterek ismeretének felhasználásával az adagolási rend kiszámításához.
Például az orvosnak ki kell választania a teofillin infúzió sebességét, valamint a további adagot, hogy fenntartsa a hatékony koncentrációt, ha a gyógyszert 12 óra, 8 óra, napi 1 alkalommal veszi be. Ismeretes, hogy a teofillin clearance-e 2,8 l/h/70 kg, a cél (hatékony) koncentráció 10 mg/l, a gyógyszer biohasznosulása 0,96.
A fenti képleteket használva a következőket kapjuk:
 Így egy körülbelül 350 mg-os adagot tartalmazó tabletta (kapszula) felírható 12 óránkénti bevételre. Nyolcórás intervallum alkalmazása esetén az adag körülbelül 233 mg, ha pedig 24 órás időközönként veszik be. , 700 mg.
Így egy körülbelül 350 mg-os adagot tartalmazó tabletta (kapszula) felírható 12 óránkénti bevételre. Nyolcórás intervallum alkalmazása esetén az adag körülbelül 233 mg, ha pedig 24 órás időközönként veszik be. , 700 mg.
Mint ismeretes, a kinetika (a görög kinētikуs szóból - mozgásba állítás) a mozgás tudománya, a farmakokinetika pedig a gyógyszer különböző módon történő beadása után a szervezetben történő „mozgásának” tudománya.
A klinikai farmakokinetika a klinikai farmakológia olyan része, amely a gyógyszerek emberi szervezetbe való bejutásának, felszívódásának, eloszlásának, biotranszformációjának és a szervezetből történő kiválasztódásának módjait vizsgálja.
Annak érdekében, hogy nyomon követhető legyen a gyógyszer mozgása a szervezetben, a vérplazmában lévő koncentrációját hosszú ideig tartó adagolás után korszerű fizikai-kémiai elemzési módszerekkel (kromatográfiás, immunológiai stb.) határozzák meg. A kapott adatok alapján grafikont készítünk a gyógyszer (vagy metabolitja) koncentrációjának a gyógyszer beadása utáni időtől való függéséről. Ezt a grafikont farmakokinetikai görbének nevezik (2-1. ábra).
ábra szerint. 2-1 ez egyértelmű hatóanyag, a gyógyszerformából felszabaduló, fokozatosan felszívódik a szisztémás véráramba (1. grafikon), eloszlik a szervek és szövetek között, elér egy bizonyos maximális értéket, különböző biotranszformációs szakaszokon megy keresztül és kiválasztódik a szervezetből. A következő főbb farmakokinetikai folyamatokat különböztetjük meg: felszívódás (abszorpció), eloszlás, asszociáció a plazmafehérjékkel, biotranszformáció (metabolizmus), kiválasztás (eltávolítás).
Rizs. 2-1. Farmakokinetikai görbe (1 - egy felszívódó adagolási formához, például orálisan; 2 - egy intravaszkuláris beadásra szánt adagolási formához, például intravénásan).
Meg kell jegyezni, hogy ezek a folyamatok a szervezetben nem egymás után, hanem egyidejűleg mennek végbe, i.e. a gyógyszer egy része felszívódik és már metabolizálódik, egy része még mindig fehérjéhez kötődik, a másik pedig még csak felszívódik. Ebben a tekintetben rendkívül nehéz leírni a gyógyszer szervezetben, minden szervben és szövetben történő eloszlásának folyamatának minden részletét. A farmakokinetika matematikai leírása lehetővé teszi, hogy a testet egy vagy több izolált permeábilis membránrész (kamra) formájában képzeljük el, amelyben a gyógyszer eloszlik, és áthalad egyik kamrából a másikba. A kamerák koncepciója feltételes, hiszen nincs mögötte anatómiailag korlátozott tér. Ezt a fajta modellezést kamramodellezésnek nevezik. A központi kamrának általában a vérplazmát, annak alkotóelemeit és a jól ellátott szerveket (szív, tüdő, máj, vese, belső elválasztású mirigyek) tekintik; perifériás - viszonylag gyengébb véráramlású szervek és szövetek (izmok, bőr, zsírszövet). Ezekben a kamrákban a gyógyszer különböző sebességgel oszlik el: gyorsabban a központi kamrában és lassabban a perifériás kamrában. A legtöbb egyszerű modell- egykamrás. Ebben az esetben a gyógyszer beadása után koncentrációja monoexponenciális törvény szerint csökken. A lineáris kinetika törvényeinek megfelelően a kamrában lévő gyógyszer mennyiségének változási sebessége arányos a kamrában lévő mennyiségével.
Bevezetés
A farmakokinetika a klinikai farmakológia része, amely a beadási módokat, a biotranszformációt, a vérfehérjékkel való kommunikációt, a gyógyszerek eloszlását és kiválasztását vizsgálja.
Az egyik fő mutató, amely meghatározza farmakológiai hatás, a hatóanyag koncentrációja a receptor területén, de egy teljes szervezet körülményei között lehetetlen megállapítani. Kísérletileg bebizonyosodott, hogy a legtöbb esetben összefüggés van a gyógyszer vérbeli koncentrációja és más biológiai folyadékokban és szövetekben lévő tartalma között.
Főbb farmakokinetikai paraméterek
A gyógyszer farmakokinetikai paramétereinek meghatározásához a vérben lévő tartalmát tanulmányozzák. A gyógyszer vérbe jutásával és a szervezetből való eltávolításával kapcsolatos megfelelő információk megszerzése érdekében a vérplazma gyógyszertartalmát hosszú időn keresztül folyadék- vagy gáz-folyadék kromatográfiás módszerekkel, radioimmun ill. enzim immunológiai vizsgálatok, spektrofotometriás módszer. A kapott adatok alapján grafikont (farmakokinetikai görbét) készítünk, amely az abszcissza tengelyen a vizsgálati időt, az ordináta tengelyen pedig a gyógyszer koncentrációját a vérplazmában jelzi.
A gyógyszer minden szervben és szövetben történő eloszlási folyamatának részletes leírásának bonyolultsága miatt a testet hagyományosan egy vagy több részként (kamraként) ábrázolják, amelyet egy áteresztő membrán választ el, amelyben a gyógyszer eloszlik. Ezt a fajta modellezést kamramodellezésnek nevezik. A központi kamrát általában vérnek és jól ellátott szerveknek tekintik (szív, tüdő, máj, vese, belső elválasztású mirigyek, a perifériás kamrát kevésbé intenzíven ellátott szerveknek és szöveteknek tekintik (izmok, bőr, stb.); zsírszövet). Ezekben a kamrákban a gyógyszer különböző sebességgel oszlik el: gyorsabban a központi kamrában, lassabban a perifériás kamrában. A legegyszerűbb az egykamrás modell, amikor feltételezzük, hogy a gyógyszer beadása után koncentrációja monoexponenciális törvény szerint csökken. A lineáris kinetika törvényeinek megfelelően a kamrában lévő gyógyszer mennyiségének változási sebessége arányos a kamrában lévő mennyiségével.
A látszólagos eloszlási térfogat (Vd) a testfolyadék hipotetikus térfogata, amely a gyógyszer teljes mennyiségének (beadott dózis) egyenletes eloszlásához szükséges a vérplazmában lévőhöz hasonló koncentrációban. Ezt a mutatót l/kg-ban mérik. Intravénás beadás esetén az eloszlási térfogat megegyezik a gyógyszer dózisának és a vérben lévő kezdeti koncentrációjának arányával.
- * Magas értékek Az eloszlási térfogat azt jelzi, hogy a gyógyszer aktívan behatol a biológiai folyadékokba és szövetekbe. Sőt, ha egy gyógyszert aktívan megköt például a zsírszövet, a vérben lévő koncentrációja szinte azonnal nagyon lecsökkenhet, és a megoszlási térfogat több száz litert is elér, meghaladva a tényleges testnedvek térfogatát. Ezért ezt a mutatót látszólagos eloszlási térfogatnak nevezik.
- *Az elosztás mennyisége számos tényezőtől függ.
- - Fizikai-kémiai jellemzők A drogok (molekulatömeg, ionizációs és polaritási fok, vízben és zsírokban való oldhatóság) befolyásolják a membránokon való áthaladását.
- - Fiziológiai tényezők(életkor, nem, a zsírszövet teljes mennyisége a szervezetben). Például időseknél és újszülötteknél a Vd csökken.
- - Patológiás állapotok, különösen a máj-, vesebetegségek, a szív-érrendszer(CCS).
Maximális koncentráció (Cmax) és a maximális koncentráció kialakulásának ideje (Tmax). Amikor egy gyógyszer a szisztémás keringésbe kerül (extravascularis beadás esetén), koncentrációja fokozatosan növekszik, eléri a Tmax pillanatnyi értéket (Cmax), majd csökkenni kezd.
* Ha a felszívódási folyamat lineáris (a folyamat sebessége egyenesen arányos a rendszerben lévő gyógyszerek mennyiségével), akkor ennek a folyamatnak a sebességét a felszívódási állandóval (kabs) jellemezzük, órákban mérve és a féléven keresztül számolva. felszívódási periódus (T1/2abs) - az az idő, amely alatt a gyógyszer beadott dózisának 1 /2-a felszívódik.