Это преждевременное возбуждение желудочков, которое связано с патологией развития проводящей системы сердца. Это не заболевание, а клиническое проявления врождённой патологии, связанной с образованием ещё во внутриутробном развитии, дополнительных путей, проводящих импульс от предсердия к желудочкам. Не стоит путать с экстрасистолией , которая характеризуется внеочередным сокращением желудочка, связанного с образованием внеочередного импульса в любой части проводящей систем вне синусового узла. Синдром предвозбуждения желудочков может быть причиной развития экстрасистолии, мерцательной аритмии, трепетания желудочков и так далее.
В медицинской литературе встречается два мнения относительно данного синдрома. Одни считают, что наличие дополнительных проводящих путей, вне зависимости от проявления, уже является синдромом предвозбуждения желудочков. Другая же часть авторов, склоняются к тому, что если не наблюдается развитие пароксизмальной тахикардии, то патологию стоит называть лишь как “феноменом предвозбуждения”. И соответственно синдромом можно считать только в том случае, если возникают пароксизмы наджелудочковой тахикардии.
Патогенез синдромов предвозбуждения желудочков
Причина синдрома в аномальном распространении по миокарду импульса возбуждения в следствии наличия дополнительных патологических проводящих путей, полностью или частично «шунтирующих» АВ-узел. Это приводит к тому, что часть или весь миокард начинает возбуждаться раньше, недели при обычном распространении от по АВ-узла к пучку Гиса и дальше по его ножкам.
На сегодня известны следующие патологические проводящие АВ-пути:
- Пучки Кента, в том числе и скрытые ретроградные. Они связывают предсердие и желудочки.
- Пучки Джеймса. Они соединяют синусовый узел и нижнюю область АВ-узла.
- Волокна Махейма. Они соединяют АВ-узел или с межжелудочковой перегородки в правой её области или с правой ножкой пучка Гиса. Иногда волокна Махейма соединяют ствол пучка Гиса и правый желудочек.
- Тракт Брешенманше. Он соединяет правое предсердие и ствол пучка Гиса.
Виды синдрома предвозбуждения желудочков
В клинической кардиологии на сегодня различают два вида синдрома:
- Синдром Вольффа-Паркинсона-Уайта (WPW-синдром или Wolff-Parkinson-White). Характеризуется укороченным интервалом в P-Q(R), незначительная деформация и уширение QRS и образование дополнительной дельта-волны, а также изменение зубца Т и сегмента ST. Чаще встречается при аномальном АВ-проведении пучка Кента. Существует целый ряд типов данного вида синдрома, а также интермиттирующий (перемежающийся) и транзиторный (переходящий). Некоторые авторы, вообще выделяют аж до десяти подтипов WPW-синдрома.
- Синдром Клерка-Леви-Кристеско (синдром короткого интервала PQ или CLC-синдром). В английских источниках его именуют как синдром Lown-Ganong-Levine (LGL-синдром). Характеризуется также укороченным интервалом P—Q(R), но без изменения комплекса QRS. Обычно возникает при аномальном АВ-проведении пучка Джеймса.
Симптомы
Сам синдром никак себя не проявляет. Человек может жить долго и счастливо, даже не подозревая, что у него есть патологический дополнительный проводящий путь в сердечной мышце. Первые признаки могут возникнуть в любом возрасте, как правило на фоне другого заболевания, при чём не обязательно миокарда. Это могут быть, например любые инфекционные болезни.
У пациентов с CLC-синдромом часто первые проявления начинаются с пароксизмальных тахикардий .
WPW-синдром проявляется следующими нарушениями ритма:
Наджелудочковые реципрокные тахикардии, которые с возрастом переходят в мерцательную аритмию. Данное проявления WPW-синдрома встречается у 80% пациентов.
- Пароксизмальных тахиаритмии встречаются у 75% пациентов с WPW-синдромом.
- Фибрилляция встречается у 15-30% людей с WPW-синдромом.
- Трепетание или мерцание предсердий встречается у 5% пациентов.
Диагностика синдромов предвозбуждения желудочков
Основным методом диагностики является ЭКГ. Обычно уже на ЭКГ чётко видны характерные признаки. Для определения вида и типа синдрома назначают:
- ЭКГ с нагрузкой,
- Мониторирование по Холтеру ,
- Монополюсное поверхностное ЭКГ-картирование,
- Эхокардиография,
- ЭФИ (электрофизиологическое исследование миокарда),
- ЧПСС (чреспищеводное стимулирование миокарда).
Лечение
Если пароксизмы отсутствуют, то лечение не проводится. В других случаях используют медикаментозное лечение, которое должен назначит специалист в зависимости от ситуации. Препараты всегда подбираются индивидуально с учётом патологии, сопутствующих заболеваний и других индивидуальных особенностей организма.
Если медикаментозная терапия не приносит желаемого эффекта, назначают электроимпульсную терапию, то есть проведение электрокардиостимуляции.
Из радикальных методов лечения используют радиочастотную катетерную абляцию с целью деструкции патологических путей. На сегодня это единственный метод, который в 95 % случаев имеет положительный результат. Конечно есть и свои осложнения, а смертность составляет 1% из всех случаев. Перед абляцией пациент должен обязательно пройти ЭФИ.
Прогноз
Сильно зависит от тяжести синдрома, наличии осложнений и побочных заболеваний. Но даже в самых тяжёлых случаях, проведение качественной высокочастотной абляции во многом улучшает прогноз. Многое также зависит от больного: здоровый образ жизни, выполнение всех рекомендаций врача, своевременное обращение к специалисту.
Признаки предвозбуждения желудочков обнаруживаются на ЭКГ у 0,15% людей, обычно в отсутствие органического поражения сердца. У 7-10% этих больных имеется аномалия Эбштейна, дополнительные пути проведения при ней нередко множественные. Синдромы предвозбуждения желудочков чаще встречаются у мужчин, с возрастом их распространенность уменьшается, но вероятность пароксизмальных тахикардий у таких больных растет.
У 50-60% больных имеются жалобы на сердцебиение, тревожность, одышку, боль или стеснение в груди и обмороки. Примерно у четверти таких больных жалобы со временем исчезают. Если жалоб нет до 40 лет, то в дальнейшем их появление маловероятно. Дополнительные пути проведения, не проявляющиеся на ЭКГ, редко вызывают симптомы.
Этиология
Большую роль, по-видимому, играет наследственность: дополнительные пути чаще встречаются у родственников больных с синдромами предвозбуждения желудочков.
Патогенез
Чаще всего при синдромах предвозбуждения желудочков возникает ортодромная тахикардия (80-85% случаев), у 15-40% больных имеются пароксизмы мерцательной аритмии, у 5% - трепетание предсердий. Желудочковая тахикардия не характерна.
Синдром WPW
При этом синдроме имеется дополнительный проводящий путь, лежащий вне проводящей системы сердца, который соединяет предсердия с желудочками. По этому пути возбуждение из предсердий распространяется на желудочки в обход АВ-узла. Раньше эти дополнительные пути называли пучками Кента. Возбуждение распространяется на желудочки и по дополнительному пути, и через АВ-узел, достигая желудочков почти одновременно. Это приводит к предвозбуждению желудочков, представляющему собой по сути сливной комплекс: часть миокарда желудочков возбуждается через дополнительный путь (на ЭКГ при этом появляется δ-волна), а весь остальной миокард возбуждается обычным образом.
Если антеградное проведение осуществляется только через дополнительный путь, то предвозбуждение захватывает весь миокард желудочков и комплекс QRS в результате оказывается широким. Проведение по дополнительным путям может быть быстрым, но рефрактерный период у них обычно длиннее, чем у АВ-узла. Ортодромная тахикардия часто начинается с предсердной экстрасистолы, которая попадает на фазу рефрактерности дополнительного пути и проводится на желудочки по уже вышедшему из состояния рефрактерности АВ-узлу. На ЭКГ при этом формируется комплекс QRS без δ-волны. Возбуждение распространяется по желудочкам, застает дополнительный путь вышедшим из состояния рефрактерности и распространяется по нему обратно на предсердия. У небольшой, но все же значимой (5-10%) части больных имеется несколько дополнительных путей проведения.
Постоянная реципрокная тахикардия из АВ-соединения
Постоянная реципрокная тахикардия из АВ-соединения - это очень стойкая наджелудочковая тахикардия с участием необычного скрытого дополнительного пути проведения.
Этот дополнительный путь своими свойствами напоминает АВ-узел: проведение в нем происходит с затуханием. Чем чаще он возбуждается,тем медленнее становится проведение. Дополнительный путь обычно располагается в задней части межпредсердной перегородки и обеспечивает ретроградное проведение с желудочков на предсердия. Проведение по этому пути происходит с затуханием, а потому медленно. При длительном течении постоянная тахикардия из АВ-соединения может приводить к аритмогенной кардиомиопатии.
Волокна Махейма
Волокна Махейма - еще одна разновидность дополнительных путей проведения. Они могут быть двух видов: предсерднопучковыми и пучковожелудочковыми. В первом случае дополнительные пути располагаются на некотором расстоянии от АВ-узла и соединяются с правой ножкой пучка Гиса. При реципрокной тахикардии с участием волокон Махейма антеградное проведение происходит по волокнам Махейма, поэтому комплекс QRS имеет форму как при блокаде левой ножки пучка Гиса с отклонением электрической оси сердца влево. Ретроградное проведение осуществляется через АВ-узел. При пучковожелудочковых волокнах Махейма возбуждение из пучка Гиса идет по этим волокнам в обход дистальных отделов проводящей системы.
Диагностика
ЭКГ-критерии синдрома WPW
- Короткий интервал PQ(< 120 мс)
- Расширенный комплекс QRS (> 120 мс) с деформацией его восходящей части в некоторых отведениях (δ-волна) и нормальной конечной частью
- Отклонение сегмента ST и зубца Т в сторону, противоположную δ-волне и основному направлению комплекса QRS
Чаще всего при синдроме WPW наблюдается тахикардия с узкими комплексами QRS и частотой 150-250 в минуту. Она начинается и кончается одномоментно. Локализацию дополнительных путей можно оценить по обычной ЭКГ. По самой простой классификации все пути делят на тип А и тип В.
При синдроме WPW типа А в отведении V 1 имеется высокий зубец R. Дополнительный путь при этом расположен слева и вызывает предвозбуждение задних базальных сегментов левого желудочка.
При синдроме WPW типа В в отведении V 1 регистрируется зубец S или комплекс вида QS, а дополнительный путь располагается в правых отделах. Оценить локализацию дополнительного пути можно по форме ретроградного зубца Р, если он хорошо виден. Разработаны и более сложные алгоритмы. Однако наиболее надежно в этом отношении ЭФИ: локализацию дополнительного пути определяют при стимуляции желудочков или во время ортодромной тахикардии. В последнем случае исследование наиболее информативно, поскольку ретроградное проведение осуществляется только по дополнительному пути, тогда как при стимуляции желудочков импульс отчасти идет и через АВ-узел.
Положительный зубец Р в V 1 , во время тахикардии указывает на локализацию дополнительного пути в свободной стенке левого желудочка, а отрицательный зубец Р в V1 говорит о том, что он проходит справа.
Оценка прогноза
Наличие признаков предвозбуждення желудочков на одних ЭКГ и их отсутствие на других прогностической ценности не имеет. Напротив, появление и исчезновение предвозбуждення желудочков от комплекса к комплексу указывает на благоприятный прогноз. Данный признак можно выявить при холтеровском мониторинге ЭКГ или при нагрузочной ЭКГ-пробе. Такое непостоянное предвозбуждение желудочков говорит о том, что дополнительный путь не способен к быстрому АВ-проведению, поэтому риск внезапной смерти мал. Однако и постоянное предвозбуждение желудочков не обязательно указывает на высокий риск внезапной смерти. Оценка риска в этой группе больных затруднена. Поскольку наибольшую опасность при синдромах предвозбуждения желудочков представляет мерцательная аритмия, возможность ее спровоцировать может иметь наибольшее прогностическое значение. Спровоцировать мерцательную аритмию можно с помощью чреспищеводной ЭКС, однако лучший метод оценки риска -ЭФИ.
Лечение
Купирование тахикардии
При нестабильной гемодинамике или очень плохой переносимости пароксизма проводят электрическую кардиоверсию. В остальных случаях возможно медикаментозное лечение.
При узких комплексах QRS пытаются снизить проводимость в АВ-узле. Начинают с ваготропных приемов. Из лекарственных средств обычно эффективны аденозин и верапамил, можно использовать и амиодарон. Весьма эффективна предсердная ЭКС, чреспищеводная или эндокардиальная. Если приходится прибегать к электрической кардиоверсии, начинают с разрядов небольшой энергии, но обычно электрической кардиоверсии не требуется.
При широких комплексах QRS рекомендуется использовать прокаинамид в/в (кроме того, может быть эффективно в/в введение амиодарона , флекаинида , соталола и пропафенона , но в США из этих препаратов для в/в введения существует только амиодарон).
Лидокаин, антагонисты кальция, бета-адреноблокаторы и дигоксин использовать не следует, поскольку их эффективность невысока; кроме того, они могут увеличить частоту сокращения желудочков и вызвать желудочковую тахикардию. При неэффективности медикаментозного лечения прибегают к электрической кардиоверсии. Энергия разряда должна быть не менее 200 Дж.
После деструкции дополнительного пути проведения часто исчезают не только реципрокные тахикардии, но и пароксизмы мерцательной аритмии, если до этого они возникали.
Профилактика тахиаритмии
В отсутствие жалоб риск внезапной смерти мал, поэтому медикаментозное лечение или деструкция дополнительных путей в этом случае не нужны. Исключение составляют больные, у которых случаи внезапной смерти были в семье, спортсмены и те, чья работа связана с опасностью для самих себя и окружающих (например, летчики). При наличии жалоб, а также при пароксизмах мерцательной аритмии или остановке кровообращения в анамнезе риск внезапной смерти высок. Эти больные требуют дополнительного обследования.
Медикаментозное лечение
Медикаментозное лечение возможно при высоком риске, но в отсутствие жалоб, при расположении дополнительных путей рядом с АВ-узлом (в этом случае катетерная деструкция может привести к АВ-блокаде), а также при высоком риске инвазивного лечения. В качестве монотерапии используют амиодарон, соталол, флекаинид и пропафенон. Эти препараты замедляют проведение как в АВ-узле, так и в дополнительном пути проведения. Иногда сочетают блокаторы АВ-проведения (антагонисты кальция, бета-адреноблокаторы) с препаратами, действующими на дополнительный путь проведения (антиаритмические средства класса Iа).
Радиочастотная катетерная деструкция
Эффективность метода составляет 85-98% и зависит от локализации дополнительного пути. Рецидивы возникают у 5-8% больных. Катетерную деструкцию используют при высоком риске внезапной смерти, при неэффективности или непереносимости медикаментозного лечения, а также при работе, сопряженной с опасностью (например, у летчиков).
Литература
1. Б.Гриффин, Э.Тополь «Кардиология» М. 2008
2. John R. Hampton «The ECG in practice» Fourth edition, 2003
Нарушения ритма сердца считаются важной кардиологической проблемой, поскольку нередко осложняют течение и ухудшают прогноз многих заболеваний и являются одной из самых частых причин внезапной смерти.
Особый интерес как клиницистов, так и электрофизиологов вызывает синдром преждевременного возбуждения желудочков (СПВЖ), который в одних случаях, при отсутствии клинических проявлений, может быть электрокардиографической находкой, а в других – сопровождаться опасными для жизни тахиаритмиями.
Несмотря на успехи, достигнутые в изучении СПВЖ, вопросы его диагностики, тактики ведения больных и лечения остаются актуальными и в настоящее время.
Определение. Классификация
СПВЖ (синдром предвозбуждения, преэкситации, preexcitation syndrome) – это ускоренное проведение импульса возбуждения от предсердий к желудочкам по дополнительным аномальным проводящим путям. В результате часть миокарда или весь миокард желудочков начинают возбуждаться раньше, чем при обычном распространении возбуждения по атриовентрикулярному узлу, пучку Гиса и его ветвям.
Согласно рекомендациям группы экспертов ВОЗ (1980) преждевременное возбуждение желудочков, не сопровождающееся клинической симптоматикой, называют "феноменом предвозбуждения", а в случае, когда имеются не только электрокардиографические признаки предвозбуждения, но и развиваются пароксизмы тахиаритмии, – "синдромом предвозбуждения".
Анатомическим субстратом СПВЖ служат пучки специализированных мышечных волокон вне проводящей системы сердца, способные проводить электрические импульсы к разным участкам миокарда, вызывая их преждевременное возбуждение и сокращение.
Дополнительные предсердно-желудочковые соединения классифицируют по их расположению относительно фиброзных колец митрального или трикуспидального клапанов, типу проводимости (декрементный тип – нарастающее замедление проведения по дополнительному пути в ответ на увеличение частоты стимуляции – или недекрементный), а также по их способности на антеградное, ретроградное или сочетанное проведение. Обычно дополнительные проводящие пути имеют быстрое недекрементное проведение, аналогичное таковому в нормальной ткани проводящей системы Гиса–Пуркинье и миокарда предсердий и желудочков.
В настоящее время известно несколько видов аномальных проводящих путей (трактов):
- предсердно-желудочковый (Кента), соединяющий миокард предсердий и желудочков в обход атриовентрикулярного узла;
- атрионодальный (Джеймса), расположенный между синоатриальным узлом и нижней частью атриовентрикулярного узла;
- нодовентрикулярный (Махейма), связывающий атриовентрикулярный узел (или начало пучка Гиса) с правой стороной межжелудочковой перегородки или разветвлениями правой ножки пучка Гиса;
- атриофасцикулярный (Брешенмаше), соединяющий правое предсердие с общим стволом пучка Гиса.
Существуют также и другие дополнительные пути проведения, в том числе "скрытые", способные проводить электрический импульс ретроградно от желудочков к предсердиям. У небольшой (5–10 %) части больных имеется несколько аномальных путей проведения.
В клинической практике выделяют:
- синдром Вольфа–Паркинсона–Уайта (синдром WPW), обусловленный наличием пучков Кента;
- синдром Клерка–Леви–Кристеско (синдром CLC, синдром укороченного интервала Р-Q (R)), обусловленный наличием пучка Джеймса.
Электрокардиографические проявления СПВЖ зависят от степени преэкситации и постоянства проведения по дополнительным путям. В связи с этим выделяют следующие варианты синдрома:
- манифестный СПВЖ (на ЭКГ постоянно имеются признаки предвозбуждения);
- интермиттирующий (преходящий) СПВЖ (на ЭКГ признаки предвозбуждения имеют преходящий характер);
- латентный СПВЖ (ЭКГ в обычных условиях нормальная, признаки предвозбуждения появляются только в период пароксизма тахикардии или при провокации – физической нагрузке, электрофизиологическом исследовании (ЭФИ), вагусных или медикаментозных пробах);
- скрытый (на стандартной ЭКГ изменения не выявляются из-за проведения возбуждения по дополнительным путям только ретроградно).
Распространенность
По разным данным, распространенность СПВЖ в общей популяции составляет примерно 0,15 %. При этом пароксизмы тахиаритмий возникают у каждого второго пациента (в 80–85 % случаев – ортодромная тахикардия, 20–30 % – фибрилляция предсердий (ФП), 5–10 % – трепетание предсердий и антидромная тахикардия). Скрытый СПВЖ выявляют у 30–35 % больных.
СПВЖ – это врожденная аномалия, но клинически может проявиться в любом возрасте, спонтанно или после какого-либо заболевания. Обычно данный синдром манифестирует в молодом возрасте. В большинстве случаев иной патологии сердца у пациентов нет. Однако описываются сочетания СПВЖ с аномалией Эбштейна, кардиомиопатиями, пролапсом митрального клапана. Существует предположение о наличии взаимосвязи между СПВЖ и дисплазией соединительной ткани.
В семьях больных, страдающих этим синдромом, был выявлен аутосомно-доминантный тип наследования дополнительных проводящих путей у родственников I, II, III степени родства с различными клинико-электрокардиографическими проявлениями.
Частота случаев внезапной смерти у пациентов с СПВЖ составляет 0,15–0,6 % в год. Почти в половине случаев остановка сердца у лиц с СПВЖ – его первое проявление.
Исследования больных с СПВЖ, перенесших остановку сердца, ретроспективно определили ряд критериев, с помощью которых можно выявить лиц с повышенным риском внезапной смерти. К ним относят наличие следующих признаков:
- укороченного интервала R-R – менее 250 мс во время спонтанной или индуцированной ФП;
- симптоматической (гемодинамически значимой) тахикардии в анамнезе;
- множественных дополнительных путей;
- аномалии Эбштейна.
История
ЭКГ с укороченным интервалом P-Q и одновременно уширенным комплексом QRS впервые описали A. Cohn и F. Fraser в 1913 г. Единичные подобные случаи были описаны в последующем и некоторыми другими авторами, однако в течение многих лет причиной такой картины ЭКГ считалась блокада ветвей пучка Гиса.
В 1930 г. L. Wolff, J. Parkinson и P. White представили доклад, в котором электрокардиографические изменения такого типа рассматривали как причину пароксизмальных нарушений ритма сердца. Эта работа дала основание для проведения всесторонних исследований, направленных на выяснение патогенеза указанных изменений на ЭКГ, названных в последующем синдромом Вольфа–Паркинсона–Уайта.
Спустя два года M. Holzman и D. Scherf предположили, что в основе синдрома WPW лежит распространение импульса возбуждения по дополнительным предсердно-желудочковым путям. В 1942 г. F. Wood предоставил первое гистологическое подтверждение наличия мышечного соединения между правым предсердием и правым желудочком, выявленного при аутопсии больного 16 лет с эпизодами пароксизмальной тахикардии в анамнезе.
Несмотря на эти данные, активный поиск альтернативных механизмов развития синдрома продолжался до 1970-х, когда ЭФИ и хирургические методы лечения подтвердили теорию дополнительных проводящих путей.
Патогенез
Проведение импульсов от предсердий к желудочкам при СПВЖ происходит одновременно по нормальной проводящей системе сердца и по дополнительному пути. В проводящей системе на уровне атриовентрикулярного узла всегда наблюдается некоторое замедление проведения импульсов, не характерное для аномального тракта. В результате этого деполяризация определенного участка миокарда желудочков начинается преждевременно еще до распространения импульса по нормальной проводящей системе.
Степень предвозбуждения зависит от соотношения скоростей проведения в нормальной проводящей системе сердца, прежде всего в атриовентрикулярном узле, и в дополнительном пути проведения. Увеличение скорости проведения по дополнительному проводящему пути или замедление скорости проведения по атриовентрикулярному узлу приводят к повышению степени предвозбуждения желудочков. В некоторых случаях деполяризация желудочков может быть целиком обусловлена проведением импульсов по дополнительному пути. В то же время при ускорении проведения импульсов по атриовентрикулярному узлу или замедлении проведения по дополнительному пути степень аномальной деполяризации желудочков снижается.
Основное клиническое значение дополнительных путей проведения состоит в том, что они нередко включаются в петлю кругового движения волны возбуждения (re-entry) и способствуют таким образом возникновению наджелудочковых пароксизмальных тахиаритмий.
При СПВЖ чаще всего встречается ортодромная реципрокная наджелудочковая тахикардия, при которой импульс проводится антеградно по атриовентрикулярному узлу, а ретроградно – по дополнительному проводящему пути. Пароксизм ортодромной наджелудочковой тахикардии характеризуется частыми (140–250 в 1 мин), лишенными признаков преэкситации нормальными (узкими) комплексами QRS. В ряде случаев после комплекса QRS наблюдаются инвертированные зубцы Р, что указывает на ретроградную активацию предсердий.
При антидромной наджелудочковой тахикардии импульс циркулирует в противоположном направлении: антеградно – по аномальному проводящему пути, ретроградно – по атриовентрикулярному узлу. Пароксизм антидромной наджелудочковой тахикардии у больных с СПВЖ проявляется на ЭКГ частым регулярным ритмом (150–200 в 1 мин) с желудочковыми комплексами по типу максимально выраженной преэкситации (QRS і 0,11 с), после которых иногда выявляются инвертированные зубцы Р.
У 20–30 % пациентов с СПВЖ возникают пароксизмы ФП, при которых в результате антеградного проведения по дополнительному пути большого числа предсердных импульсов частота сокращений желудочков (ЧСЖ) может превышать 300 в 1 мин.
Клиника
Во многих случаях СПВЖ протекает бессимптомно и выявляется только электрокардиографически. У 50–60 % больных имеются жалобы на приступы сердцебиений, одышку, боль или дискомфорт в груди, чувство страха и обмороки. Особую опасность при СПВЖ приобретают пароксизмы ФП, поскольку они сопровождаются большой ЧСЖ, гемодинамическими нарушениями и нередко могут трансформироваться в фибрилляцию желудочков. В таких случаях у больных не только наблюдают синкопальные состояния, но и имеется высокий риск внезапной смерти.
Независимыми факторами риска развития ФП у пациентов с СПВЖ являются возраст, мужской пол и наличие в анамнезе синкопальных состояний.
Диагностика
Основным методом диагностики СПВЖ является ЭКГ.
При синдроме WPW на фоне синусового ритма выявляют укорочение интервала P-Q (<0,12 с) и D-волну (пологий наклон в первые 30–50 мс) на восходящей части зубца R или нисходящей части зубца Q, комплекс QRS обычно расширен (і0,11 с). Характерно также отклонение сегмента SТ и зубца Т в сторону, противоположную D-волне и основному направлению комплекса QRS.
Электрокардиографическими признаками синдрома CLC являются укорочение интервала P-Q (R), продолжительность которого не превышает 0,11 с, отсутствие в составе комплекса QRS дополнительной волны возбуждения – D-волны, наличие неизмененных (узких) и недеформированных комплексов QRS (за исключением случаев сопутствующей блокады ножек или ветвей пучка Гиса).
При СПВЖ, обусловленном функционированием пучка Махейма, определяется нормальный интервал P-Q при наличии D-волны.
Одновременное функционирование пучков Джеймса и Махейма приводит к появлению на ЭКГ признаков, характерных для синдрома WPW (укорочение интервала P-Q (R) и наличие D-волны).
В связи с распространением в последние годы хирургических методов лечения больных с СПВЖ (деструкция аномального пучка) постоянно совершенствуются способы точного определения его локализации.
На ЭКГ местоположение пучка Кента обычно определяют по направлению начального моментного вектора деполяризации желудочков (первых 0,02–0,04 с), который соответствует времени формирования аномальной D-волны. В тех отведениях, активные электроды которых располагаются непосредственно над участком миокарда, возбуждающимся аномально за счет пучка Кента, регистрируется отрицательная D-волна. Это указывает на распространение раннего аномального возбуждения в сторону от активного электрода данного отведения.
Особый практический интерес представляют возможности метода пространственной вектор-электрокардиографии, позволяющего с высокой точностью установить локализацию дополнительных проводящих путей.
Более подробную, по сравнению с данными ЭКГ, информацию о местоположении дополнительных путей проведения можно получить с помощью магнитокардиографии.
Однако наиболее достоверными и точными являются методы внутрисердечного ЭФИ, в частности эндокардиальное (предоперационное) и эпикардиальное (интраоперационное) картирование. При этом с помощью сложной методики определяют область наиболее ранней активации (предвозбуждения) миокарда желудочков, которая соответствует локализации дополнительного аномального пучка.
Лечение
У больных с бессимптомным течением СПВЖ лечения обычно не требуется. Исключение составляют лица, в семейном анамнезе которых были случаи внезапной смерти, спортсмены и те, чья работа связана с опасностью для самих себя и окружающих (например, водолазы и летчики).
При наличии пароксизмов наджелудочковой тахикардии лечение заключается в купировании приступов и их профилактике с помощью различных медикаментозных и немедикаментозных методов. При этом важное значение имеет характер аритмии (орто-, антидромная тахикардия, ФП), ее субъективная и объективная переносимость, ЧСЖ, а также наличие сопутствующих органических заболеваний сердца.
При ортодромной реципрокной наджелудочковой тахикардии импульс возбуждения проводится антеградно нормальным путем, поэтому ее лечение должно быть направлено на угнетение проводимости и блокаду импульсов в атриовентрикулярном узле. С этой целью используют рефлекторные вагусные пробы, которые наиболее эффективны при возможно более раннем применении.
Препаратом первого ряда для купирования ортодромной реципрокной наджелудочковой тахикардии считают аденозин, потенциальным недостатком которого является преходящее повышение возбудимости предсердий, способное провоцировать их экстрасистолию и фибрилляцию сразу же после купирования пароксизма такой тахикардии. Другим средством выбора для купирования ортодромной тахикардии при отсутствии выраженной артериальной гипотензии и тяжелой систолической сердечной недостаточности принято считать верапамил. В качестве препаратов второго ряда обычно используют b-адреноблокаторы.
При неэффективности этих средств применяют новокаинамид с целью блокады проведения через добавочный атриовентрикулярный путь. По своей безопасности и эффективности новокаинамид является препаратом выбора при лечении тахикардии с широкими комплексами QRS, когда диагноз ортодромной реципрокной наджелудочковой тахикардии вызывает сомнения.
Препаратами резерва являются амиодарон, соталол и антиаритмические препараты (ААП) 1С класса: пропафенон или флекаинид.
При антидромной реципрокной наджелудочковой тахикардии импульс проводится ретроградно через атриовентрикулярный узел, поэтому применение верапамила, дилтиазема, лидокаина и сердечных гликозидов для ее купирования противопоказано в связи со способностью данных препаратов ускорять антеградное проведение по добавочному пути и тем самым увеличивать ЧСЖ. Применение этих средств, а также аденозина может провоцировать переход антидромной наджелудочковой тахикардии в ФП. Препаратом выбора для купирования такой тахикардии является новокаинамид, при неэффективности которого используют амиодарон или ААП 1С класса.
При возникновении пароксизма ФП основной целью медикаментозной терапии является контроль частоты ритма желудочков и замедление проводимости одновременно по добавочному пути и АВ узлу. Препаратом выбора в таких случаях также является новокаинамид. Высокоэффективно и внутривенное введение амиодарона и ААП 1С класса.
Следует отметить, что применение верапамила, дигоксина и b-адреноблокаторов при ФП с целью контроля ЧСЖ у лиц с СПВЖ противопоказано из-за их способности увеличивать скорость проведения по добавочному пути. Это может перенести фибрилляцию с предсердий на желудочки.
Для профилактики пароксизмов наджелудочковых тахиаритмий, обусловленных наличием дополнительных проводящих путей, используют ААП IА, IС и III классов, обладающие свойством замедлять проведение по аномальным путям.
К немедикаментозным методам купирования приступов наджелудочковых тахиаритмий относят трансторакальную деполяризацию и предсердную (чреспищеводную или эндокардиальную) электрокардиостимуляцию, а для их профилактики – катетерную или хирургическую абляцию добавочных путей.
У больных с СПВЖ электрическую кардиоверсию применяют при всех формах тахикардии, которые сопровождаются выраженными нарушениями гемодинамики, а также при неэффективности медикаментозной терапии и в случаях, когда она вызывает ухудшение состояния больного.
Радиочастотная катетерная абляция добавочных путей является в настоящее время основным методом радикального лечения СПВЖ. Показаниями к ее выполнению являются высокий риск внезапной смерти (прежде всего наличие пароксизмов ФП), неэффективность или плохая переносимость медикаментозной терапии и профилактики приступов наджелудочковой тахикардии, а также нежелание больного принимать ААП. В случае выявления короткого эффективного рефрактерного периода аномального тракта у лиц с редкими и нетяжелыми пароксизмами аритмии, вопрос о целесообразности абляции в целях профилактики внезапной смерти решается индивидуально.
Перед катетерной абляцией выполняется ЭФИ, цель которого – подтверждение наличия дополнительного проводящего пути, определение его электрофизиологических характеристик и роли в формировании тахиаритмии.
Эффективность радиочастотной катетерной абляции высока (достигает 95 %), а летальность, связанная с процедурой, не превышает 0,2 %. Наиболее частыми серьезными осложнениями данного метода лечения являются полная атриовентрикулярная блокада и тампонада сердца. Рецидивы проведения по дополнительному пути возникают приблизительно в 5–8 % случаев. Повторная радиочастотная абляция, как правило, полностью устраняет проведение по дополнительным путям.
В настоящее время область применения хирургической деструкции добавочных путей значительно сузилась. При тех же показаниях, что и к катетерной абляции, к хирургическому лечению прибегают в случаях невозможности выполнения последней по техническим причинам или ее безуспешности, а также при необходимости проведения операции на открытом сердце в связи с сопутствующей патологией.
Литература
- Сычев О.С. Нарушения ритма сердца // Руководство по кардиологии / Под ред. В.Н. Коваленко. – К.: Морион, 2008. – С. 1059-1248, 1215-1218.
- ACC/AHA/ESC 2006 Guidelines for the management of patients with atrial fibrillation // Circulation. – 2006. – № 114. – P. 257-354.
- ACC/AHA/ESC Guidelines for the management of patients with supraventricular arrhythmias – executive summary // JACC. – 2003. – № 8. – Р. 1493-1531.
- Griffin B., Topol E. Manual of Cardiovascular Medicine. – The Lippincott Williams & Wilkins, 2004. – P. 1248.
- Hanon S., Shapiro M., Schweitzer P. Early history of the preexcitation syndrome // Europace. – 2005. – № 7. – P. 28-33.
- Keating L., Morris А., Brady W.О. Electocardiographic Features of Wolff–Parkinson–White syndrome // Emerg. Med. J. – 2003. – № 20. – Р.491-493.
Н.Т. Ватутин, Н.В. Калинкина, Е.В. Ещенко.
Донецкий национальный медицинский университет им. М. Горького;
Институт неотложной и восстановительной хирургии им. В.К. Гусака АМН Украины.
Укркардіо
Синдром WPW (синдром Вольфа-Паркинсона-Уайта)
Термин "предэкзитация" (предвозбуждение) означает, что часть миокарда желудочков или весь желудочковый миокард возбуждается синусовыми (предсерными) импульсами через дополнительные пути (ДП) с опережением по сравнению с тем, что бывает в обычных условиях, когда те же импульсы проводятся к желудочкам только через АВ узел и систему Гиса-Пуркинье. В настоящее время концепция предвозбуждения включает ряд ранее неизвестных явлений, в частности, наличие:
1) скрытых ДП, избирательно проводящих импульсы в ретроградном направлении от желудочка к предсердию (так называемые скрытые ретроградные "пучки Кента")
2) мышечных соединений между АВ узлом или стволом пучка Гиса и желудочком
3) множественных ДП и др.
Основным вариантом синдрома преждевременного возбуждения желудочков является синдром WPW.
Проведение импульсов от предсердий к желудочкам при синдроме WPW происходит одновременно по нормальной проводящей системе сердца и по пучку Кента в нормальной проводящей системе на уровне АВ - узла всегда наблюдается некоторое замедление проведения импульсов. По пучку Кента импульсы проводятся без замедления. В результате возникает преждевременное возбуждение желудочков.
Клиническое значение заключается в том, что у 40-80% больных развивается пароксизмальная наджелудочковая тахиаритмия. Наиболее частым вариантом которой является пароксизмальная реципрокная АВ - тахикардия, которая обусловлена круговым движением импульса антероградно по нормальной проводящей систем сердца, а ретроградно к предсердиям по пучку Кента, реже при синдроме WPW встречается так называемая "антидромная наджелудочковая тахикардия", при которой циркуляция импульса происходит в обратном направлении: антероградно по пучку Кента, ретроградно по нормальной проводящей системе сердца. Комплексы QRS при этой тахикардии уширены по типу максимального предвозбуждения желудочков.
У больных с синдромом WPW отмечается повышенная частота случаев фибрилляции предсердий (ФП) по сравнению с общей популяцией людей, что резко резко ухудшает вполне благоприятный прогноз. Отрицательное влияние оказывают и сочетанные с предвозбуждением желудочка врожденные или приобретенные заболевания сердца. Смертельные исходы, имеющие прямое отношение с синдрому WPW, редки. Основной механизм смерти - ФЖ, вызванная частым поступлением к желудочкам волн ФП.
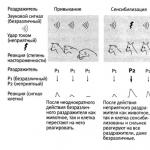
Нарушения возбудимости миокарда
Экстрасистолия
Среди возможных электрофизиологических механизмов образования экстрасистол основное значение имеют, по-видимому, два механизма:
Постдеполяризации.
В литературе можно встретить упоминание и двух других механизмов: асинхронном восстановлении возбудимости в миокарде и аномальном автоматизме (роль их не вполне ясна и нуждается в экспериментальном подтверждении).
Наджелудочковые (НЭ) и желудочковые экстрасистолы (ЖЭ) по причинам возникновения можно разделить на функциональные и органические. В функциональный класс кроме нейрогенных, можно отнести НЭ дисэлектролитного, токсического, дисгормонального, лекарственного происхождения, которые связаны со сравнительно легкими дистрофическими изменениями в миокарде и исчезают при восстановлении его метаболизма.
Среди нейрогенных различают:
Гиперадренергические,
Гипоадренергические,
Вагусные.
Гиперадренергические (гиперсимпатикотонические) НЭ узнаются по их связи с эмоциональным возбуждением ("психогенные" НЭ), с интенсивной умственной или физической работой человека, с потреблением им алкоголя, острой пищи, с курением и т.д.
Недостаток норадреналина в миокарде рассматривается как патогенетический фактор экстрасистолии у больных с алькогольно-токсической дистрофией миокарда во II, гипоадренергической, стадии. По-видимому, НЭ у некоторых спортсменов с миокардиодистрофией от хронического физического перенапряжения может быть следствием пониженного депонирования норадреналина в окончаниях симпатических нервов миокарда.
Хорошо известны аритмогенные эффекты гипокалиемии, которые возрастают при ее сочетании с анемией и дефицитом железа (чаще это бывает у женщин), с гипергликемией, задержкой ионов натрия и воды, гипопротеинемий, артериальной гипертензией. Не вызывает сомнения роль тиреотоксической дистрофии миокарда в развитии наджелудочковой экстрасистолии.
Синусовые Э большей частью связаны с хронической ИБС.
Клиническое значение НЭ определяется отрицательным влиянием на гемодинамику и способность провоцировать более тяжелые нарушения ритма: ФП (ТП), наджелудочковые (реже желудочковые) тахикардии.
ЖЭ (чаще левожелудочковые) встречаются у людей с органическими заболеваниями. В их основе могут лежать такие процессы, как ишемия, воспаление, гипертрофия миокарда от повышенной нагрузкой и др. Хотя, нельзя забывать нейрогуморальные факторы, нередко играющие роль пусковых механизмов.
Клиническое значение ЖЭ у лиц с заболеваниями сердца определяется:
Их отрицательным влиянием на кровообращение (одиночные экстрасистолические сокращения, хотя и сопровождаются понижением УО, мало изменяют МО. Частые ЖЭ, в особенности интерполированные, удваивающие общее число систол, вызывают уменьшение УО и МО сердца.
Способностью ухудшать течение стенокардии, провоцировать ЖТ и ФЖ.
ЖЭ могут долгое время быть единственным проявлением тяжелого повреждения сердца, например миокардита.
Пароксизмальная тахикардия
механизмы наджелудочковых тахикардий:
1) продольное разделение АВ узла на два электрофизиологических канала: медленный(a) и быстрый(b)
2) однонаправленная антероградная блокада быстрого канала за счет более эффективного рефрактерного периода (ЭРП)
3) возможность ретроградного проведения по быстрому каналу, клетки которого имеют сравнительно короткий ретроградный ЭРП.
Во время синусового ритма или тогда, когда электрическая стимуляция предсердий еще не достигает большой частоты, импульсы проводятся к пучку Гиса через быстрый канал АВ узла. Если же осуществляют частую стимуляцию предсердий либо их программированную стимуляцию, то в определенный момент импульс блокируется в начальной части быстрого канала (b), не вышедшего из состояния рефрактерности, но распространяется через медленный канал (a), уже восстановивший свою возбудимость после предыдущего импульса, поскольку антероградный ЭРП этого канала короче.
Медленно преодолев канал a, импульс поворачивает в пределах АВ узла к каналу b, в котором рефрактерность уже исчезла, пройдя по этому каналу в ретроградном направлении, импульс в верхней части АВ узла ("верхний общий путь") замыкает круг re-entry, т.е. совершает повторный вход в канал a. Многократное, по меньшей мере, трехкратное, воспроизведение этого процесса создает более или менее устойчивую движущуюся "круговую волну" (circus movement).
желудочковые тахикардии (ЖТ): 73-79% всех случаев ЖТ приходится на больных, заболевших острым инфарктом миокарда (острой коронарной недостаточностью) либо имеющих постинфарктную аневризму (распространенный рубец) стенки левого желудочка.
Три основных механизма ЖТ:
1. Re-entry
2. Аномальный автоматизм . ЖТ, основанная на этом механизме не вызывается программированной электрической стимуляцией желудочков. Главная их особенность - возможность индукции внутривенным введением катехоламинов либо с помощью физической нагрузки.
3. Триггерная активность - задержанные постдеполяризации. В этом случае образование эктопических импульсов происходит в виде так называемых постдеполяризаций, которые могут быть ранними или поздними (задержанными). Ранние постдеполяризации возникают во время реполяризации, поздние - в период диастолы после окончания ПД. В последнем случае сначала отмечается гиперполяризация мембраны, а затем - постдеполяризация (следовые потенциалы). ЖТ этого типа возникают при учащении синусового ритма либо под воздействием навязанного предсердного или жедудочкового ритма, когда достигается критическая длина цикла, а также под влиянием одиночных (парных) экстрасистол. Для осуществления такой реакции требуется соответствующий фон: интоксикация сердечными гликозидами, избыточное воздействие катехоламинов, накопление ионов кальция в клетках и т.д. Триггерную активность по типу поздних постдеполяризаций можно индуцировать и прервать с помощью электростимуляции.
Влияние приступов ЖТ на гемодинамику:
Резкое понижение МО сердца, возникающее в период приступа, связано с двумя причинами:
1) понижением диастолического наполнения сердца
2) уменьшением его систолического опорожнения.
Среди причин, ведущих к понижению наполнения сердца, можно выделить: укорочение диастолы во время частого ритма, неполное расслабление желудочков, повышение жесткости их стенок в период диастолы, рефлекторные влияния на величину венозного возврата крови к сердцу. К числу причин, изменяющих систолическое опорожнение сердца относятся: некоординированные сокращения различных участков мышц левого желудочка, ишемическая дисфункция миокарда, отрицательный эффект очень частого ритма, митральная регургитация крови.
Фибрилляция (мерцание) желудочков
Хаотическое асинхронное возбуждение отдельных мышечных волокон или небольших групп волокон с остановкой сердца и прекращением кровообращения.
Причины ФЖ разделяют на аритмические и внеаритмические.
К профибрилляторным аритмическим механизмам относят:
Рецидивирующие приступы устойчивой и неустойчивой ЖТ, дегенерирующей в ФЖ
- "злокачественные" ЖЭ (частые и сложные): если первая ЖЭ укорачивает рефрактерность и усиливает неоднородность процессов восстановления возбудимости в миокарде, то вторая ЖЭ приводит к фрагментированию электрической активности и в конечном счете к ФЖ
Двунаправленная веретенообразная ЖТ у больных с синдромом длинного интервала Q-Т
Пароксизмы ФП у больных с синдромом WPW и др.
Среди факторов, способных вызвать ФЖ без предшествующей тахиаритмии (1/4 всех случаев) выделяют:
Глубокую ишемию миокарду) острую коронарную недостаточность или реперфузию после ишемического периода)
Острый инфаркт миокарда
Значительную гипертрофию левого желудочка и вообще кардиомегалию
Внутрижелудочковые блокады с большим расширением комплексов QRS
Полные АВ блокады, особенно дистальные
Выраженные нарушения процесса реполяризации желудочков (изменения конечной части желудочкого комплекса) при далеко зашедшей гипокалиемии, дигитализации, массивном воздействии на сердце катехоламинов и т.д.
Закрытые травмы сердца
Воздействие на организм человека электрического тока высокого напряжения
Передозировку анестетиков в период наркоза
Гипотермию при проведении хирургических операций на сердце
Неосторожные манипуляции при катетеризации полостей сердца и др.
ФЖ служит механизмом смерти большинства сердечных больных. В одних случаях это - первичная ФЖ - следствие острой электрической нестабильности миокарда - возникающая у больных, не имеющих выраженных нарушений кровообращения (сердечной недостаточности, артериальной гипотензии, шока), в других - вторичная ФЖ при инфаркте миокарда, хронической ИБС, дилатационной кардиомиопатии, пороках сердца, миокардитах и т.д.)
Трепетание желудочков
Возбуждение миокарда желудочков с частотой до 280 в 1 мин (иногда больше 300 в 1 мин) в результате устойчивого кругового движения импульса по сравнительно длинной петле re-entry, обычно по периметру инфарцированной зоны миокарда. Как и ФЖ, ТЖ приводит к остановке сердца: сокращение его прекращаются, исчезают тоны сердца и артериальный пульс, АД падает до нуля, развивается картина клинической смерти.
Под этим термином понимается аномальное распространение волны возбуждения от предсердий к желудочкам по дополнительным аномальным проводящим путям. Эти пути короче основного А-В пути и в результате часть миокарда возбуждается раньше, а часть по АВ пути позже. Это приводит к образованию аномальных сливных комплексов QRS, иммитирущих гипертрофию желудочков, блокады ножек пучка Гиса, рубцовые изменения и острый инфаркт миокарда. Значение этих аномальных проводящих путей в том, что они включаются в цепи макро-ри-энтри и становятся причиной появления наджелудочковых пароксизмальных тахикардий.
Напомним, что имеются следующие дополнительные пути:
Пучки Кента, связывающие предсердия и миокард желудочков.
Пучки Махейма, связывающие А-В узел с правой стороной мезжелудочковой перегородки.
Пучки Джеймса, соединяющие СА узел с нижней частью А-В узла.
Пучок Брешенмаше, связывающий правое предсердие с общим стволом пучка Гиса.
Существует два ЭКГ типа синдрома предвозбуждения: синдром (феномен) Волфа-Паркинсона-Уайта (WPW), синдром (феномен) Клерк-Леви-Кристеско (CLC). Если есть синдром предвозбуждения и приступы НЖТ, то это синдром. Если НЖТ нет - феномен.
Рис. 48. Схематическое изображение допонительных проводящих путей сердца (Г.Е.Ройтберг, А.В.Струтынский, 2003г.)
Синдром (феномен) Вольфа-Паркинсона-Уайта (WPW)
При синдроме WPW волна возбуждения через пучок Кента достигает желудочки раньше, чем волна по А-В пути. Происходит возбуждение части миокарда, что дает вону дельта на восходящем колене QRS. Остальной миокард возбуждается по нормальному А-В пути.
В зависимости от расположения пучков Кента возбуждаются различные участки желудочков. Это определяет наличие трех ЭКГ типов синдрома WPW:
Тип А – пучок Кента локализуется в задне-базальной части левого желудочка. .Картина ЭКГ напоминает блокаду правой ножки пучка Гиса с высоким R в первом грудном отведении.
Тип Б – пучок локализуется в правом желудочке. Картина ЭКГ напоминает блокаду левой ножки пучка Гиса.
Тип С – левостороннее расположение пучка. ЭКГ может иметь признаки типов А и Б с волной дельта направленной вниз лефых грудных отведениях.
ЭКГ-признаки:
Интервал P-Q меньше 0,12 с.
Комплекс QRS сливной, в его составе есть волна дельта (ступенька).
Комплекс QRS расширен боле 0,10 с. и деформирован.


Рис. 49.На первой и второй ЭКГ синдром (феномен) WPW, тип А

Рис. 50. Синдром (феномен) WPW, тип Б.
Фенмен WPW может быть постоянным или преходящим. Может быть скрытым, определяемым при ЭФИ. Надо подчеркнуть, что ЭКГ при этом синдроме может напоминать блокады ножек пучка Гиса и имитировать ГЛЖ,ГПЖ, рубцовые изменения, или ОИМ.Если ОИМ происходит на фоне WPW,то обнаружить его бывает трудно.Облегчает эту ситуацию сравнение новой ЭКГ пациента со старой,снятой до приступа.
Синдром преждевременного возбуждения - CLC
Этот синдром обусловлен наличием аномального пучка Джеймса между предсердием и пучком Гиса. Волна возбуждения без задержки в А-В узле достигает пучка Гиса и возбуждение желудочков идет обычным симметричным путем.
ЭКГ признаки: укорочение P-Q менее 0,12 с. с неуширенным и не имеющим волну дельта комплексом QRS.

Рис. 51. Синдром (феномен) CLC
Еще по теме Синдром преждевременного возбуждения желудочков:
- Какова клиническая значимость преждевременного возбуждения желудочков?
- Почему при преждевременном возбуждении желудочков интервал PR укорочен?